La capacità del corpo umano di autoripararsi è straordinaria, ma non infinita. Quando una parte di osso viene danneggiata in modo molto esteso (critical-size bone defects) – ad esempio a causa di un grave trauma, un tumore o patologie degenerative – la rigenerazione naturale non è più sufficiente. In questi casi ricostruire l’osso è ancora oggi una delle sfide più difficili per i chirurghi ortopedici e maxillo-facciali.
Gli innesti ossei, cioè porzioni di osso prelevate dal paziente stesso o da un donatore, costituiscono da tempo il gold standard terapeutico, ma presentano limiti significativi, tra cui la disponibilità limitata di tessuto donatore e il rischio di complicanze.
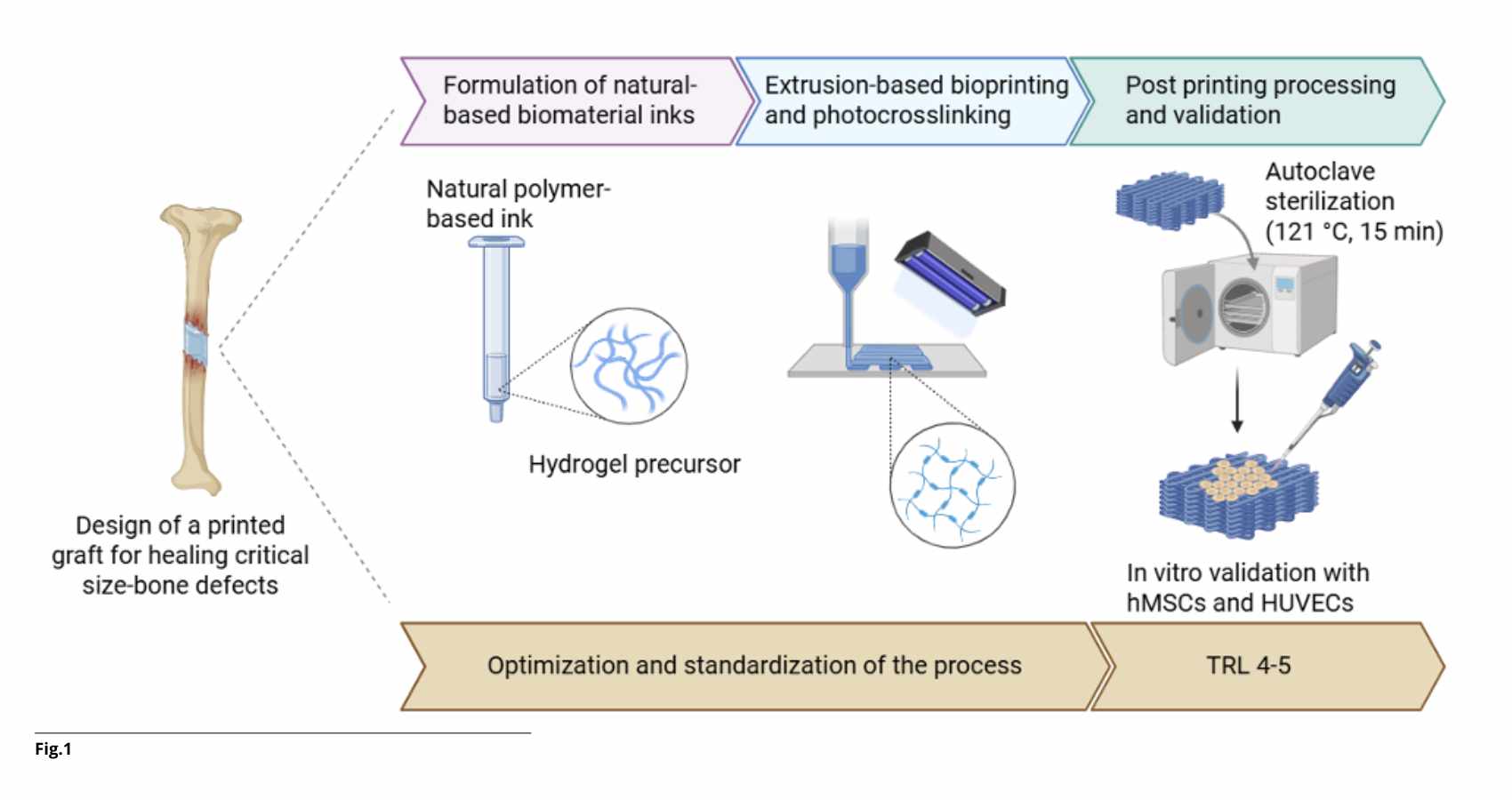
Per questo negli ultimi anni la ricerca si è concentrata sulla Bone Tissue Engineering, un campo che punta a creare sostituti dell’osso in laboratorio: strutture tridimensionali porose (scaffold) che fungono da impalcatura temporanea per guidare la formazione di nuovo tessuto e che si degradano progressivamente nel tempo.
Una delle tecnologie più promettenti per realizzarle è la biostampa 3D, che consente di fabbricare costrutti tridimensionali con un controllo spaziale estremamente preciso nella deposizione di biomateriali, molecole bioattive e cellule del paziente, replicando così l’architettura gerarchica e la micro-porosità dell’osso nativo e superando i limiti geometrici delle tecniche convenzionali.
Il principale ostacolo oggi è trovare i cosiddetti bioinchiostri: materiali che possano essere stampati facilmente ma che allo stesso tempo offrano un ambiente ideale per le cellule.
Questa ricerca nasce da una collaborazione internazionale tra il Centro BIOtech del Dipartimento di Ingegneria Industriale dell’Università di Trento (sotto la guida della prof.ssa Antonella Motta e del prof. Devid Maniglio) e il Charles Perkins Centre dell’Università di Sydney, in Australia (sotto la supervisione del prof. Anthony S. Weiss).
Il progetto è parte del programma europeo MSCA-RISE SHIFT (Shaping Innovative Products for Sustainable Tissue Engineering Strategies), che studia come utilizzare materiali naturali per sviluppare nuove soluzioni scalabili e sostenibili nella medicina rigenerativa.
L’esperienza internazionale ha confermato quanto la collaborazione globale rappresenti un pilastro della ricerca scientifica: il confronto con contesti accademici differenti non solo accelera i risultati sperimentali, ma costituisce un passaggio fondamentale nella crescita professionale del ricercatore.
Il materiale di partenza dello studio è stato la fibroina di seta (Silk Fibroin, SF), polimero naturale già noto per essere compatibile con il nostro organismo e abbastanza resistente. Il problema è che, da sola, non è facile da stampare: non forma un filamento stabile né mantiene la forma dopo la deposizione.
Per superare questi limiti è stato adottato un approccio di design multiscala, intervenendo dalla funzionalizzazione chimica nanometrica alla modulazione reologica micrometrica, fino alla validazione strutturale macroscopica.
L’ottimizzazione della stampabilità è stata ottenuta attraverso il blending con acido ialuronico metacrilato (HAMA). Grazie alla sua elevata viscosità e idrofilia, l’HAMA conferisce al sistema un comportamento shear-thinning: l’inchiostro fluisce sotto pressione durante l’estrusione e recupera rapidamente viscosità a riposo, garantendo l’indispensabile shape fidelity.
Parallelamente è stato introdotto un pre-crosslinking fisico tramite peptidi auto-assemblanti ultra-corti, aumentando le proprietà viscoelastiche del materiale prima della stampa. L’integrazione sinergica tra HAMA e peptidi ha permesso di ottenere una fedeltà di forma ottimale.
Una volta ottimizzata la stampabilità, la ricerca si è concentrata su un altro aspetto fondamentale: la bioattività specifica per il tessuto osseo. L’incorporazione di nanoidrossiapatite (HAP) – principale componente minerale dell’osso – ha trasformato l’idrogel in un composito biomimetico, migliorandone stabilità meccanica e capacità di promuovere adesione e differenziazione delle cellule staminali mesenchimali umane (hMSCs).
Durante il periodo di ricerca a Sydney, gli scaffold (le strutture stampate) sono stati ulteriormente migliorati con un rivestimento di tropoelastina, precursore dell’elastina, che ha favorito la formazione di nuovi vasi sanguigni e la crescita del tessuto osseo senza alterare le proprietà meccaniche del materiale.
In linea con i principi di sostenibilità del progetto SHIFT, è stata inoltre adottata una strategia di green chemistry, sostituendo l’idrossiapatite sintetica con una variante biogenica ottenuta da gusci di cozze – scarti alimentari valorizzati tramite sintesi meccano-chimica. I test in vitro hanno evidenziato un’attività metabolica superiore nei campioni contenenti la variante naturale, dimostrando come sostenibilità e performance biologiche possano procedere di pari passo.
Un altro obiettivo della ricerca è stato rendere il processo di stampa più affidabile e riproducibile: infatti la mancanza di standardizzazione è uno dei principali ostacoli alla traslazione clinica del bioprinting. È stato quindi sviluppato un metodo per la standardizzazione del processo di estrusione, basato su modelli matematici predittivi dei parametri di stampa. Questo contributo mira a rafforzare la riproducibilità sperimentale e a integrare le attuali normative, come la ASTM F3659.
Nel complesso, il lavoro dimostra che è possibile produrre strutture ossee stampate in 3D, bioattive e personalizzabili, utilizzando materiali naturali.
L’integrazione razionale di fibroina, acido ialuronico, idrossiapatite e tropoelastina ha permesso di soddisfare simultaneamente requisiti meccanici, reologici e biologici, aprendo la strada a soluzioni realmente traslabili dalla ricerca alla clinica.
La direzione è chiara: portare queste soluzioni dal laboratorio alla sala operatoria, è questa la traiettoria di una ricerca che dimostra come materiali naturali, competenze ingegneristiche e collaborazione internazionale possano convergere verso nuove frontiere della medicina rigenerativa.
Fig.3: Sulla sinistra esempio di Biostampa 3D di polimeri naturali e sulla destra interazione di cellule staminali (nuclei in blu e citoscheletro in verde) con scaffold ottimizzato in questo progetto.